树立百年科学难题
突破技术固有局限
小鼠作为生物医学研究中最核心的哺乳动物模型之一,百余年来广泛应用于癌症、炎症、神经退行性疾病等领域的研究。理解疾病,往往需要知道特定条件下体内每种细胞在做什么——而小鼠全身包含数百种器官与组织,每种组织中又存在多种细胞类型。能否在一次实验中,同时获取全身范围内各类细胞的基因表达状态,是生命科学领域长期面临的核心技术挑战之一。
现有技术各有局限:空间转录组学可以在保留空间位置信息的前提下测量基因表达,但检测范围有限,难以覆盖成年小鼠整体;全身成像技术可以观察形态结构,却无法获取全基因组层面的分子信息。两类方法的局限,使完整的全身分子图谱长期付之阙如。
为打破这一困境,该团队从实验技术、计算方法与人工智能应用三大领域跨学科协同推进,团队首次将单细胞分辨率的分子分析拓展至全机体尺度,不仅建立了覆盖小鼠全身的分子与细胞图谱,更探索了 AI 方法在大规模生物图像解析中的应用路径,为健康与疾病条件下的全身尺度系统性生物学研究,奠定了全新的技术和数据基础。成果发表于最新国际顶级期刊《细胞》(Cell)。芝加哥大学是该成果的第一作者单位,复旦大学为该成果的共同通讯作者单位。

《细胞》(Cell)报道截图
该研究得到国家自然科学基金、上海市科学技术委员会、小米公益基金、复旦鲲鹏昇腾孵化中心基金的资助。
论文链接:
https://doi.org/10.1016/j.cell.2026.03.006
通讯作者:
鲍峰(复旦大学,fbao@fudan.edu.cn)、Nicolas Chevrier(芝加哥大学)
同期报道: 《 Science 》
https://www.science.org/content/article/milestone-research-method-measures-gene-activity-across-whole-mice
打造全新研究平台
首绘全鼠体分子图谱
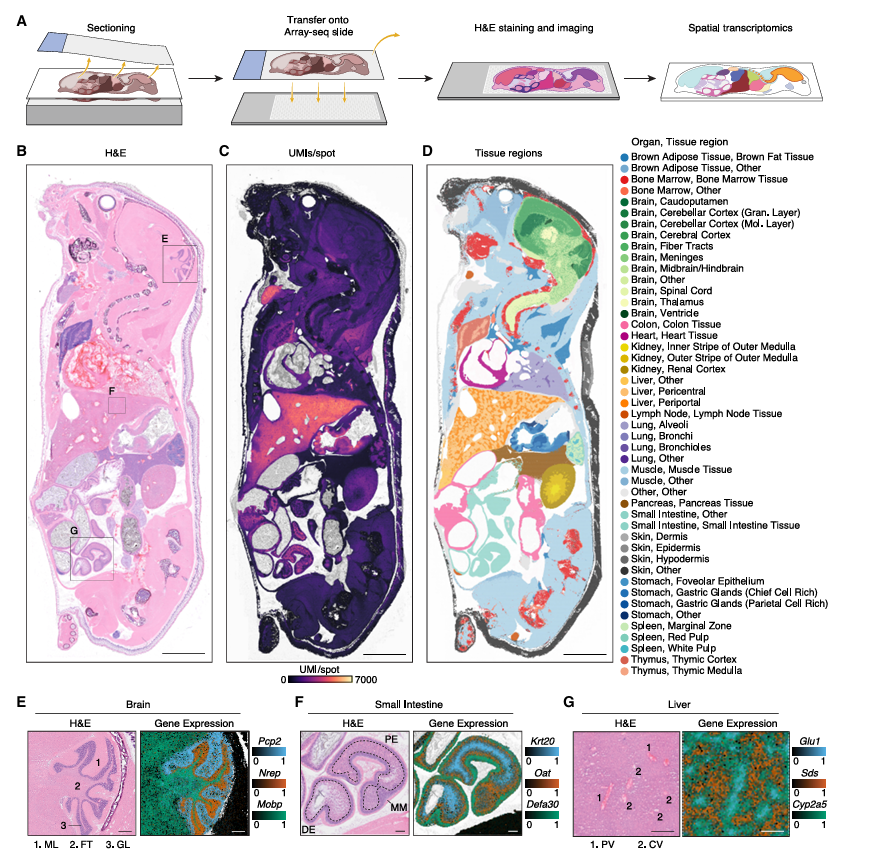
研究团队自主开发了适用于整只小鼠切片的大尺寸空间转录组平台 Array-seq,将整体小鼠冷冻切片精准铺展于约 11 平方厘米的载片上,设置约 97 万个检测位点,实现了单次实验覆盖小鼠全身 16 个器官系统的技术突破。
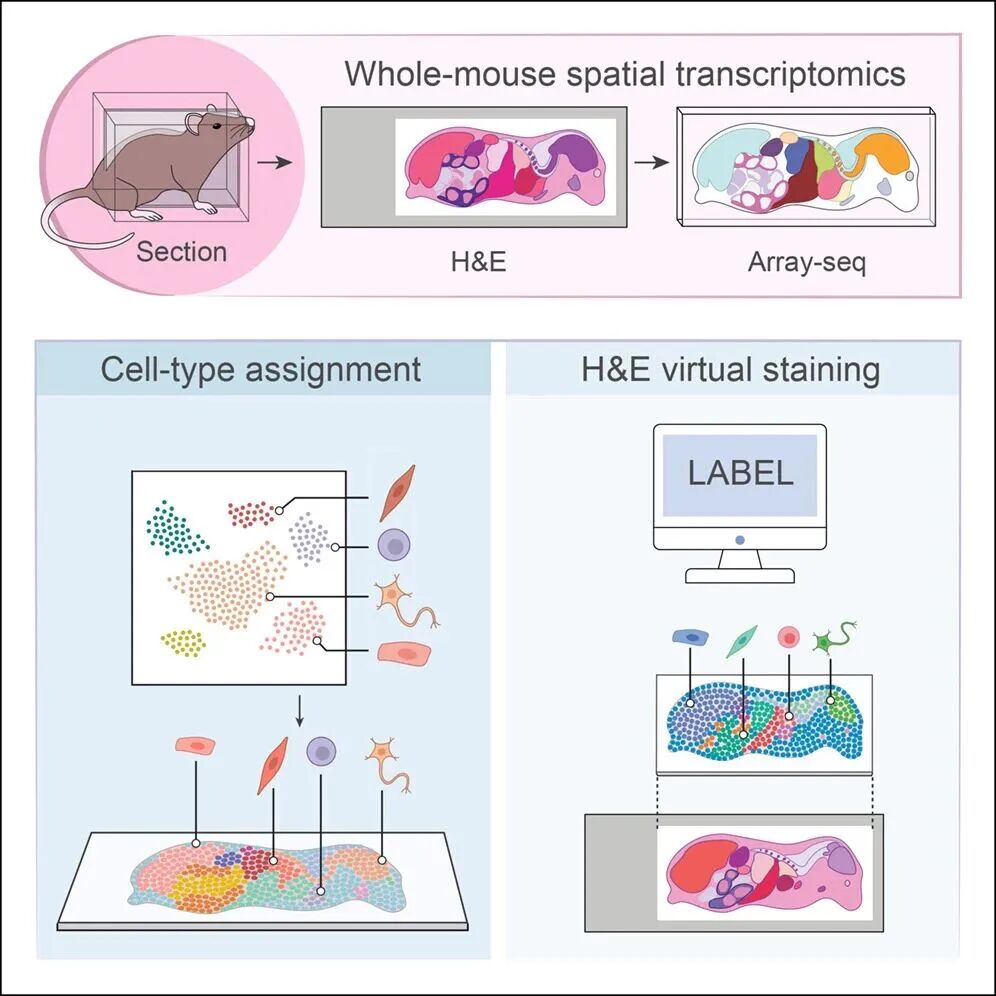
为实现单细胞分辨率的精准分析,团队整合了包含5900 万个单细胞、466 项单细胞 RNA 测序研究的海量参考数据集,在小鼠全身截面约 500 万个细胞核中,成功识别出379 种细胞类型,首次实现全小鼠体尺度的单细胞分辨率空间定位。
人类首次在全鼠尺度观测全器官生物分子分布
这一成果让人类首次在完整机体尺度上观察到小鼠全器官的生物分子分布图景,一幅清晰、精准的全小鼠体 “分子地图” 就此诞生。
AI4S:AI 赋能图谱解析
实现生物图像智能标注
构建全小鼠体空间转录组图谱本身是一项规模浩大的系统工程,涉及整体动物切片、大规模测序与海量数据处理。如何将这套数据资源转化为可低成本、高效复用的分析工具,是释放其科学价值的关键所在。鲍峰课题组主导开发了LABEL模型,使研究者无需重复上述复杂流程,仅凭常规组织切片图像即可完成全身细胞类型的自动注释,将这套全身分子知识体系推广至更广泛的研究场景。这一工作是信息科学与生命科学交叉融合的具体实践,也是复旦大学未来信息创新学院在AI赋能生命科学方向上的重要探索。相关模型训练得到了复旦大学CFFF(Computing for the Future at Fudan)智能计算平台的算力支持。
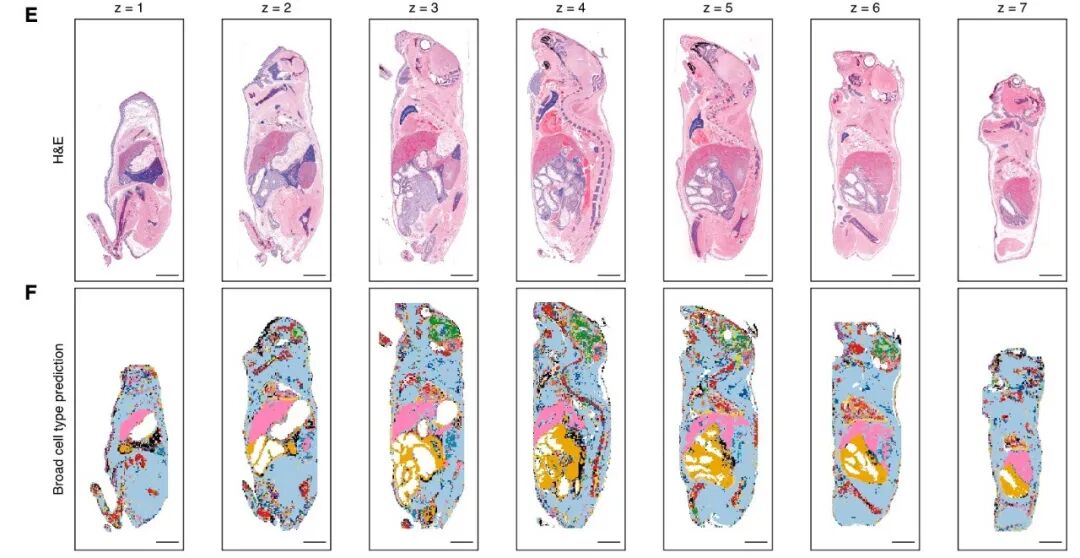
该模型以本研究构建的全身细胞图谱为核心参考,覆盖多个器官系统的495 种细胞类型,形成了从器官到细胞亚类的完整参考体系。借助 LABEL 模型,研究人员可将常规 H&E 染色切片的组织形态与分子身份精准关联,实现全身范围内器官、组织及细胞类型的自动标注,大幅减少对额外基因测序的依赖,显著提升研究效率。
实验评估显示,仅使用约 3% 的数据训练后,LABEL 模型在 16 个器官上的平均预测准确率达 90%,展现出优异的实用性和泛化能力。
树立领域研究新标杆
为生物医学研究开辟新方向
过去百年,生物医学研究积累了大量单个基因、细胞和器官的研究成果,但不同器官与细胞在整体机体层面的协同机制,始终缺乏系统性的观测手段。鲍峰团队提出的全新研究框架,实现了 “单细胞分辨率” 与 “整体机体尺度” 的完美结合,为解决这一问题提供了关键方案。
这一成果也得到了国际领域内专家的高度评价:波士顿儿童医院暨哈佛医学院副教授 Jeffrey Moffitt 称其为空间转录组学领域的 “技术里程碑”,并指出其研究规模前所未有;耶鲁大学生物医学工程学教授 Rong Fan 认为,该平台的独特价值在于能单次实验捕捉多器官、多细胞类型的全身协同响应;欧洲分子生物学实验室课题组长 Detlev Arendt 则表示,该方法延伸至不同物种后,将为器官与组织演化研究提供全新参考。
目前,这一研究框架已为肿瘤转移、全身性炎症、系统性代谢调控等涉及多器官协调的研究方向,提供了全新的观测视角。随着不同疾病模型、时间点与遗传背景数据的持续积累,其作为生物医学研究基础性资源的价值将进一步凸显。
 地址:上海市淞沪路2005号复旦大学交叉二号楼B6001室 200438
地址:上海市淞沪路2005号复旦大学交叉二号楼B6001室 200438
 电话:021-31242602
电话:021-31242602  Email:cse@fudan.edu.cn
Email:cse@fudan.edu.cn
版权所有: 2019年 复旦大学通信科学与工程系

关注微信号

